Calculadora de Gramos a Moles
Convierte la masa en gramos a moles con la fórmula n = m / M. Ingresa la masa de la muestra y la masa molar para obtener un resultado limpio de estequiometría.
Calculadora de Gramos a Moles
Usa gramos dividido por la masa molar para encontrar moles.
¿Qué Es Un Mol En Química?
Un mol (mol) es la unidad base SI para la cantidad de sustancia. Un mol contiene exactamente 6.022 × 10²³ entidades elementales, ya sean átomos, moléculas o iones. Este número fijo se llama constante de Avogadro (NA).
Piénsalo como una "docena", pero astronómicamente más grande. Una docena siempre significa 12 objetos; un mol siempre significa 6.022 × 10²³ objetos. Lo que cambia entre sustancias es la masa de ese mol, y eso es lo que te dice la masa molar.
Este concepto une dos mundos: la escala microscópica de átomos y el mundo macroscópico de gramos que puedes medir en una balanza de laboratorio. Sin el mol, la estequiometría, la preparación de soluciones y el equilibrio de ecuaciones químicas serían imposibles de hacer prácticamente.

Hecho clave: El mol fue definido de modo que un mol de átomos de carbono-12 pese exactamente 12 gramos. Esta es la razón por la que las unidades de masa atómica y la masa molar son numéricamente iguales.
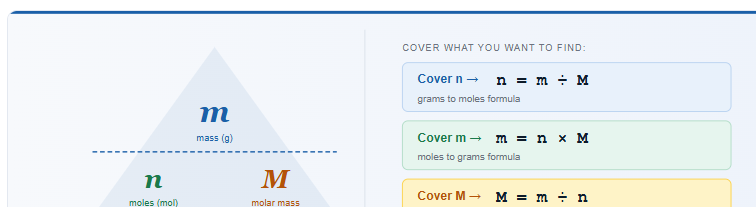
La Fórmula de Gramos a Moles (n = m ÷ M)
La relación entre masa, moles y masa molar se expresa en una ecuación, el fundamento de todo cálculo de estequiometría en química:
Reorganizando obtienes el conjunto completo de tres fórmulas:
| Encontrar | Fórmula | Cuándo Usar |
|---|---|---|
| Moles (n) | n = m ÷ M | Tienes masa, quieres moles |
| Masa en gramos (m) | m = n × M | Tienes moles, quieres masa |
| Masa molar (M) | M = m ÷ n | Tienes masa y moles |
Cómo Convertir Gramos a Moles — Paso a Paso
Ejemplos Trabajados: Gramos a Moles (y De Vuelta)
Sigue estas soluciones completas para entender el método, no solo la respuesta.
¿Cuántos moles hay en 36 g de agua?
→ Masa molar de H₂O = 2(1.008) + 15.999 = 18.015 g/mol
→ n = 36 ÷ 18.015
¿Cuál es la masa de 0.5 mol de NaCl?
→ Masa molar de NaCl = 22.99 + 35.45 = 58.44 g/mol
→ m = 0.5 × 58.44
¿Cuántos moles hay en 1 kg de glucosa?
→ Conversión: 1 kg = 1,000 g
→ Masa molar = 6(12.01) + 12(1.008) + 6(16.00) = 180.16 g/mol
→ n = 1000 ÷ 180.16
Una muestra de 180.16 g contiene 2.0 mol de un compuesto. ¿Cuál es su masa molar?
→ M = m ÷ n = 180.16 ÷ 2.0
Conteo de partículas de moles: Multiplica moles por el número de Avogadro: N = n × 6.022 × 10²³. Por ejemplo, 2 mol de agua = 1.204 × 10²⁴ moléculas.
Tabla de Referencia de Masa Molar para Sustancias Comunes
Busca rápidamente la masa molar de compuestos comúnmente utilizados en tareas, preparación de laboratorio y problemas de estequiometría.
| Sustancia | Fórmula | Masa Molar (g/mol) | Tipo de Enlace |
|---|---|---|---|
| Agua | H₂O | 18.015 | Covalente |
| Cloruro de sodio (sal de mesa) | NaCl | 58.44 | Iónico |
| Dióxido de carbono | CO₂ | 44.01 | Covalente |
| Glucosa (azúcar en sangre) | C₆H₁₂O₆ | 180.16 | Covalente |
| Amoníaco | NH₃ | 17.03 | Covalente |
| Ácido sulfúrico | H₂SO₄ | 98.08 | Covalente |
| Carbonato de calcio | CaCO₃ | 100.09 | Iónico |
| Etanol | C₂H₅OH | 46.07 | Covalente |
| Hidróxido de sodio | NaOH | 40.00 | Iónico |
| Ácido clorhídrico | HCl | 36.46 | Covalente |
| Gas oxígeno | O₂ | 32.00 | Elemental |
| Carbono | C | 12.01 | Elemental |
Errores Comunes Que Cometen Los Estudiantes (Y Cómo Evitarlos)
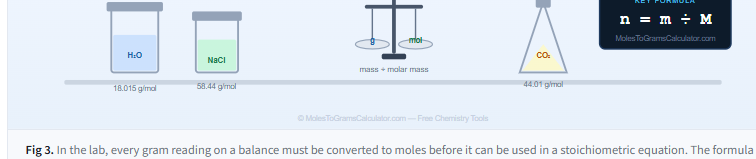
Por Qué La Conversión de Gramos a Moles Es Importante En La Química Real
Estequiometría y Ecuaciones Balanceadas
Las ecuaciones químicas balanceadas expresan reacciones en proporciones molares, no proporciones en gramos. Antes de calcular el rendimiento o pesar un reactivo, cada masa debe convertirse a moles.
Preparación de Soluciones (Molaridad)
Cuando un protocolo requiere una solución 0.1 M, eso significa 0.1 mol de soluto por litro. Para pesar la cantidad correcta, conviertes esos 0.1 moles en gramos usando m = n × M.
Aplicaciones Farmacéuticas e Industriales
Cada ingrediente activo farmacéutico se mide con precisión molecular. Los fabricantes convierten un recuento de mol objetivo en gramos para determinar la masa por lote. La misma lógica rige la producción de fertilizantes, química de polímeros y análisis ambiental.
Nota de laboratorio: Un error en esta conversión no solo afecta tu calificación. En un laboratorio real puede arruinar un experimento completo. Siempre verifica trabajando hacia atrás.
Preguntas Frecuentes
Haz clic en cualquier pregunta para expandir la respuesta.
¿Cómo conviertes gramos a moles?
Divide la masa en gramos por la masa molar en g/mol: n = m ÷ M. Por ejemplo, 36 g de agua ÷ 18.015 g/mol = 2.00 mol.
¿Qué es la masa molar y cómo la calculo?
La masa molar es la masa de un mol de una sustancia. Calcúlala sumando las masas atómicas de cada átomo en la fórmula.
¿Qué es el número de Avogadro y por qué es importante?
El número de Avogadro es 6.022 × 10²³ partículas por mol. Conecta gramos medibles con conteos de partículas.
¿Pueden los moles ser un decimal o fracción?
Sí. Los moles a menudo aparecen como decimales, como 0.25 mol o 2.50 mol.
¿Cuál es la diferencia entre masa molar y peso molecular?
Son numéricamente similares para muchos problemas de química, pero la masa molar usa g/mol mientras que el peso molecular es usualmente adimensional.
¿Cómo manejo compuestos hidratados como CuSO₄·5H₂O?
Incluye las moléculas de agua en la masa molar. Suma la masa de CuSO₄ más cinco moléculas de agua.
Mi masa está en miligramos. ¿Cómo uso esta calculadora?
Convierte miligramos a gramos primero dividiendo por 1,000.
¿Cuántos moles hay en 100 g de agua?
100 g ÷ 18.015 g/mol = 5.55 mol de agua.
Puntos Clave
- 1 mol = 6.022 × 10²³ partículas.
- Gramos a moles: n = m ÷ M.
- Moles a gramos: m = n × M.
- La masa molar es la suma de todas las masas atómicas en la fórmula.
- Siempre confirma que la masa está en gramos antes de calcular.
- Esta conversión es el fundamento de todo problema de estequiometría.
Comparte Esta Calculadora
Envía la calculadora de gramos a moles a un compañero, socio de laboratorio o grupo de estudio.
Otras Calculadoras de Química
Usa estas calculadoras para problemas relacionados de estequiometría, soluciones y composición.